
近日,新疆医科大学的科研团队相继在国际权威期刊上发表重要成果:
1 第一附属医院(第一临床医学院)脊柱外科团队与武汉协和医院合作,在《先进功能材料》上发表了创新成果。
2 第一附属医院(第一临床医学院)心律失常诊疗中心研究团队,在《今日材料生物》发表研究成果,为心律失常防控提供了“从结构到功能”的系统解决方案。
3 基础医学院李梦佳副教授作为共同作者,在《白血病》上揭示了白血病耐药的新机制,为临床治疗带来新希望。
这三项成果标志着学校在脊髓损伤修复、心肌梗死后心肌损伤修复和白血病的耐药机制研究等前沿领域取得关键突破。我校正以扎实的原创能力,诠释了争创“双一流”的底气与实力。
破解脊髓损伤修复难题:
一枚“智能贴片”让神经再生成为可能
脊髓损伤——这一中枢神经系统的严重创伤,是造成患者终生瘫痪的“元凶”。传统治疗手段难以逆转损伤局部的氧化应激和炎症风暴,受损神经元不断丢失,轴突再生几乎停滞。
新疆医科大学第一附属医院(第一临床医学院)脊柱外科团队与武汉协和医院合作,在国际权威期刊《Advanced Functional Materials》(《先进功能材料》)上发表了创新成果,提出了一种仿生多功能水凝胶贴片。该材料以天然来源的镁掺杂碳点纳米水凝胶贴片为核心,负载橙汁外泌体,构建“主动修复”的智能体系。
该文章由新疆医科大学第一附属医院(第一临床医学院)骨科中心脊柱外科胡宇坤,高书涛,荀传辉为共同第一作者,盛伟斌教授为通讯作者,武汉协和医院骨科马良为共同通讯作者完成。

本研究围绕“缓解氧化应激+调节炎症微环境+抑制神经元死亡”的目标,构建了一种仿生多功能水凝胶体系。该体系应用于损伤区域时,不仅展现出优异的生物黏附与靶向递送能力,同时具备持续清除活性氧、下调炎症信号通路、抑制神经元铁死亡并促进细胞外基质重构的综合效应。
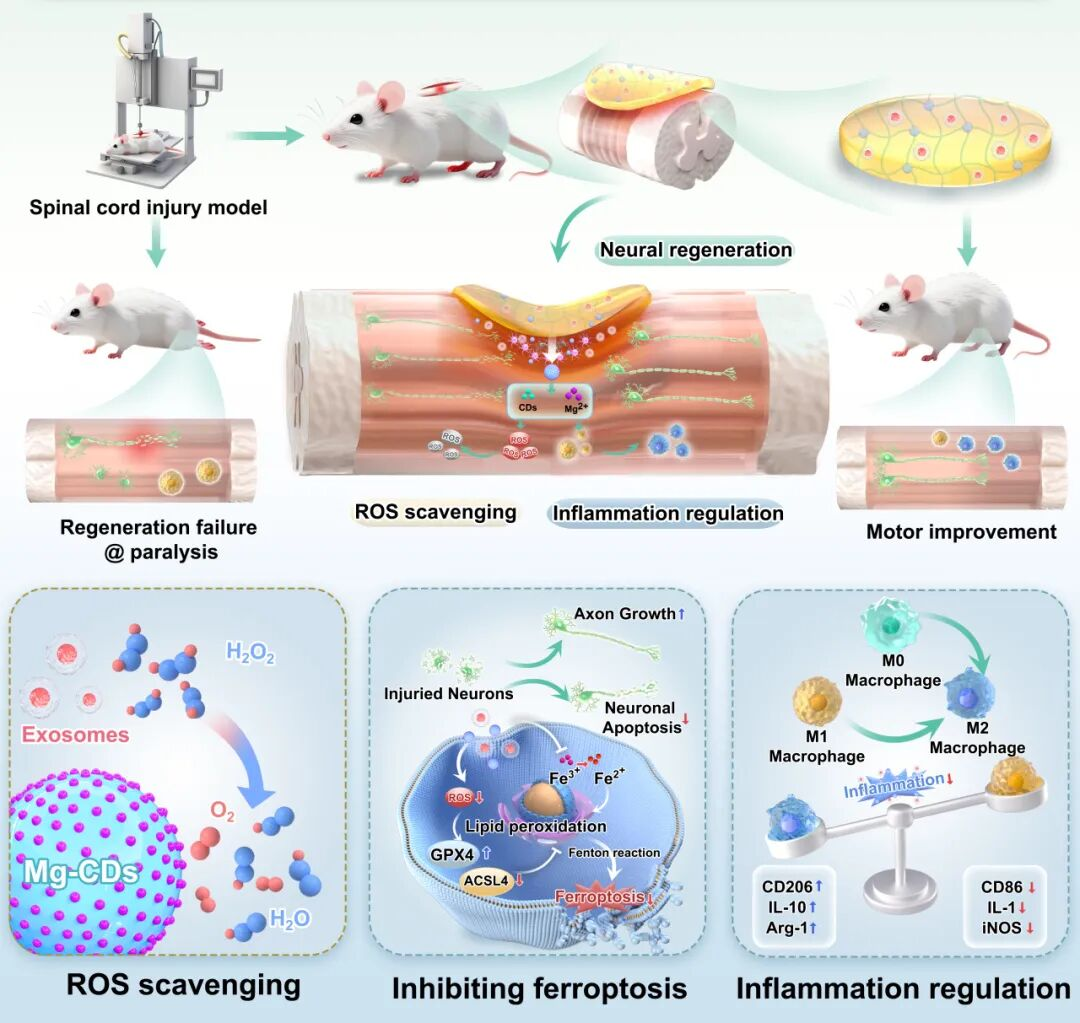
如同在损伤的脊髓上敷上一片“智能创可贴”——不仅能黏附在受损区域,还能持续清除有害的氧化物、调节过度激活的炎症反应、抑制神经元的“铁死亡”,引导并促进轴突生长。
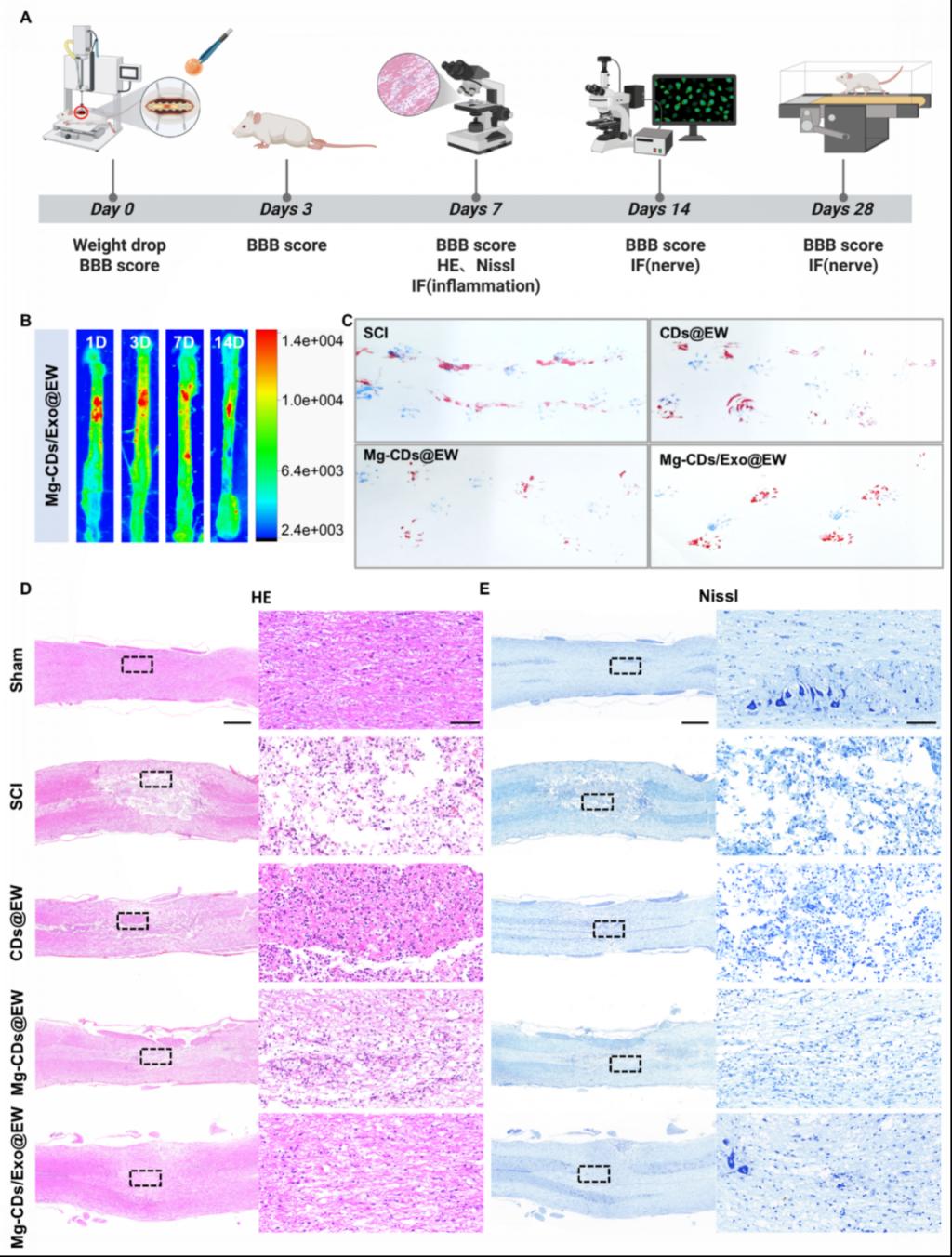
新医研究团队在大鼠脊髓损伤模型中植入该贴片后,发现损伤局部的氧化应激及炎症反应得到显著缓解,组织学提示,组织空洞与胶质瘢痕明显减小,且有效支持了轴突再生与神经环路重建,大鼠的运动功能得到显著改善。转录组与代谢组学分析进一步证实,Mg-CDs能够协同Exo中类黄酮与维生素C等成分,通过多通路阻断神经炎症进程并重塑免疫微环境。这一策略为后续脊髓损伤的临床治疗与转化提供了创新的理论与实验支持。未来,新医研究团队将继续围绕脊髓损伤后的病理微环境重构核心瓶颈,推动“外源性修复+内源性再生诱导”策略向更高层级的临床应用转化研究迈进。
精准修复心肌损伤:
为心肌梗死后心肌修复提供新方案
目前的临床研究中,遇到心肌梗死后“结构损伤”与“电功能失衡”的问题,通常难以实现阶段性修复。当前的临床治疗大多集中于再灌注或药物干预,虽然能部分改善心功能,但对梗死区电传导的中断及心律失常风险,依然缺乏有效的干预手段。
新疆医科大学第一附属医院(第一临床医学院)心律失常诊疗中心的研究取得了重要进展,相关研究成果发表于国际权威期刊《Materials TodayBio》(《今日材料生物》)。该文章由心脏起搏电生理科汤宝鹏教授、周贤惠教授指导,博士研究生宋洁为第一作者。
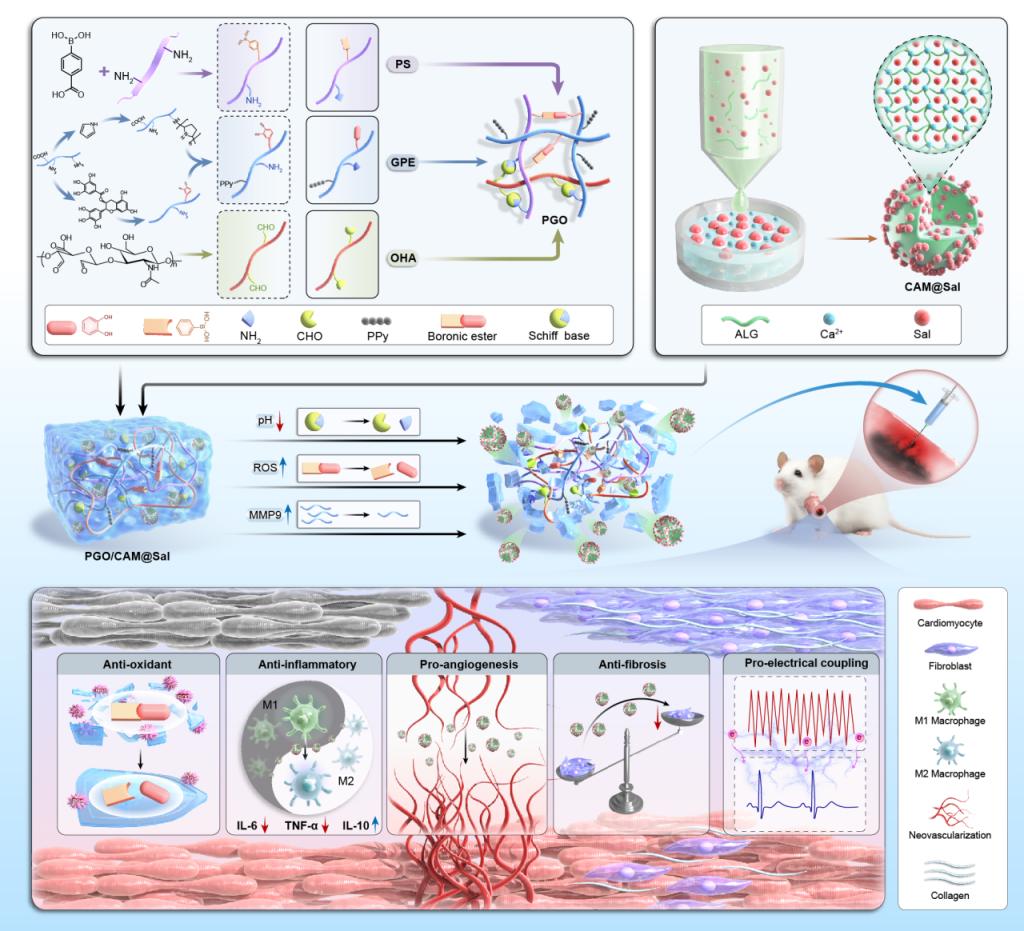
依托心脏起搏与电生理领域对“电传导重建与节律稳定”的临床需求,研究团队提出“导电结构重建+阶段响应递药+微环境多通路调控”的一体化修复策略,构建了可注射智能导电水凝胶体系PGO/CAM@Sal。

该体系设计了一套能随病情变化“智能适应”的修复方案。它构建了一种含有导电材料(聚吡咯)和特殊响应机制的水凝胶,这种水凝胶既能像“电桥”一样,连通心肌梗死区域中断的电信号,恢复心脏跳动的同步性;又能根据梗死区不断变化的pH、氧化应激和酶(MMP9)水平,按需释放负载在微球中的中药成分(红景天苷)。
通过这种双重作用——恢复导电通路和精准释放药物——该体系不仅能从物理上支撑受损的心壁,更能从“电活动”和“生物功能”两个层面协同作用,促进心肌组织的有效修复。
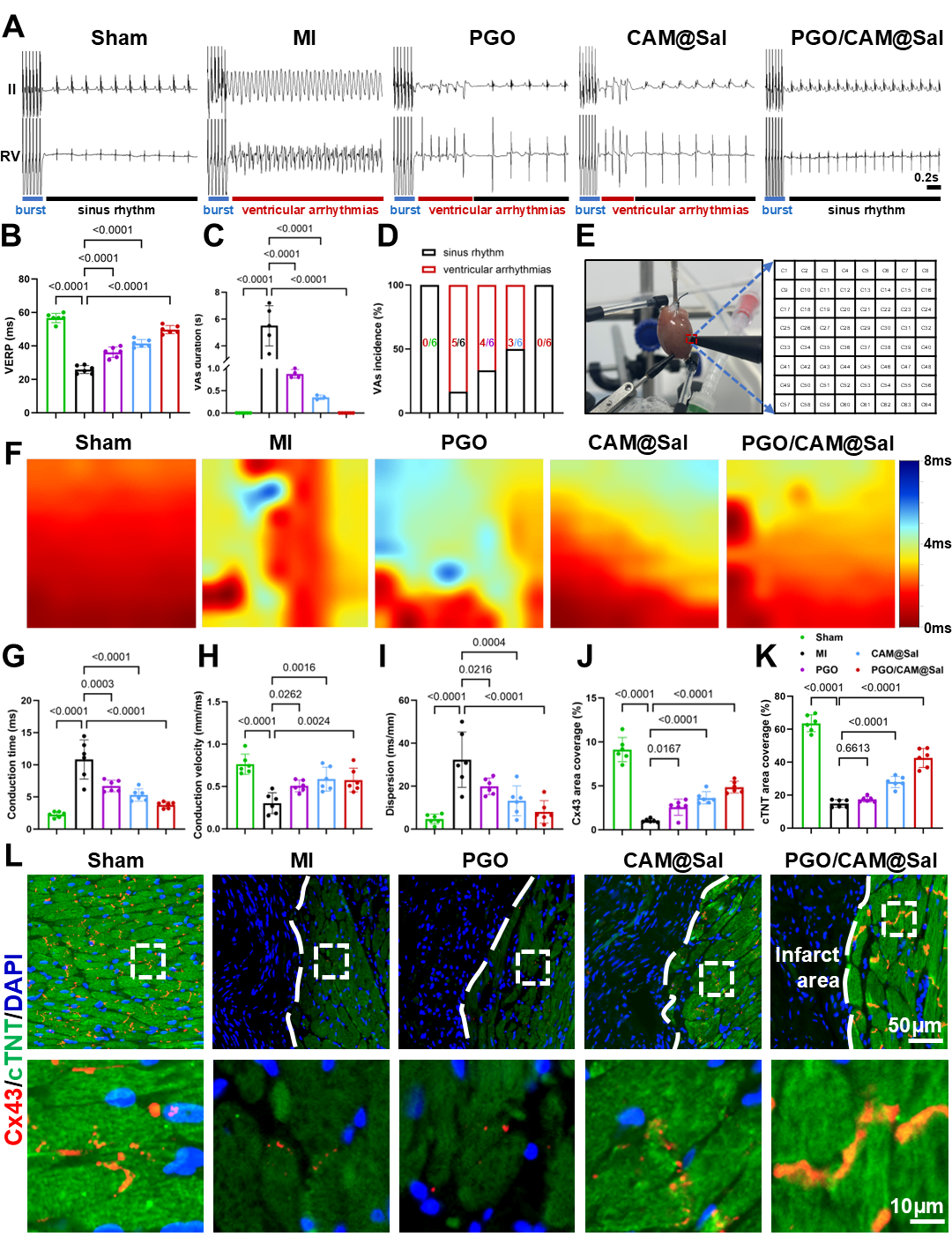
电生理功能测试进一步验证了该材料的优势。在活体心脏实验中PGO/CAM@Sal能有效纠正心脏不应期的异常,缩短心律失常的持续时间,并降低其发生频率。在离体心脏组织中,该材料能修复梗死区域中断的电信号通路,加快电信号传导速度,并减少信号传导的不均匀性,从而抑制折返性心律失常(一种常见且危险的心律失常类型)的发生。此外,实验还发现,与心脏电信号传导密切相关的Cx43蛋白表达显著增加,表明细胞间的“通信连接”得到了重建。这些结果共同说明,该体系不仅能直接改善细胞间的电偶联,还能通过改善心肌的微环境和细胞连接,从根本上帮助心脏恢复稳定的电生理状态。
进一步的转录组学和实验验证表明,PGO/CAM@Sal可能通过调控Mmp12/Cybb轴,协同影响炎症反应、氧化应激、钙信号转导等相关通路,实现对心肌重构的多通路整合调控,所构建的PGO/CAM@Sal智能导电水凝胶,不仅为心肌梗死后电传导重建提供了新思路,也为心律失常防控提供了“从结构到功能”的系统解决方案。
揭示白血病耐药新机制:
精准狙击最棘手的难题
白血病治疗中,耐药是导致复发和死亡的最棘手问题之一。很多患者初始用药效果良好,但一段时间后药物失灵,肿瘤卷土重来。原因何在?
新疆医科大学基础医学院李梦佳副教授作为共同作者,与上海海洋大学、上海交通大学医学院等团队合作,在权威期刊《Leukemia》(《白血病》影响因子13.4,中科院1区)上发表研究成果,首次发现了一个隐藏在白血病细胞中的“耐药开关”。
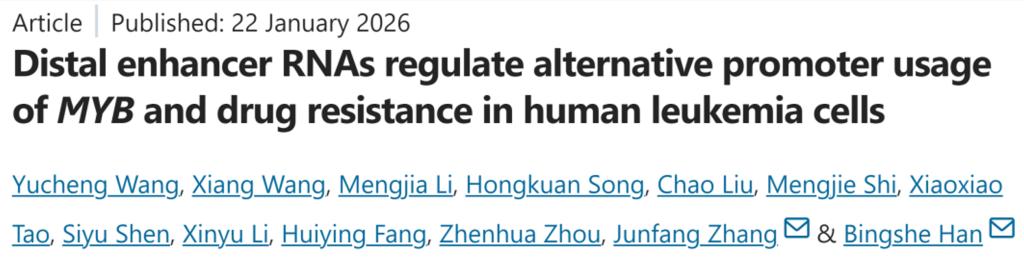
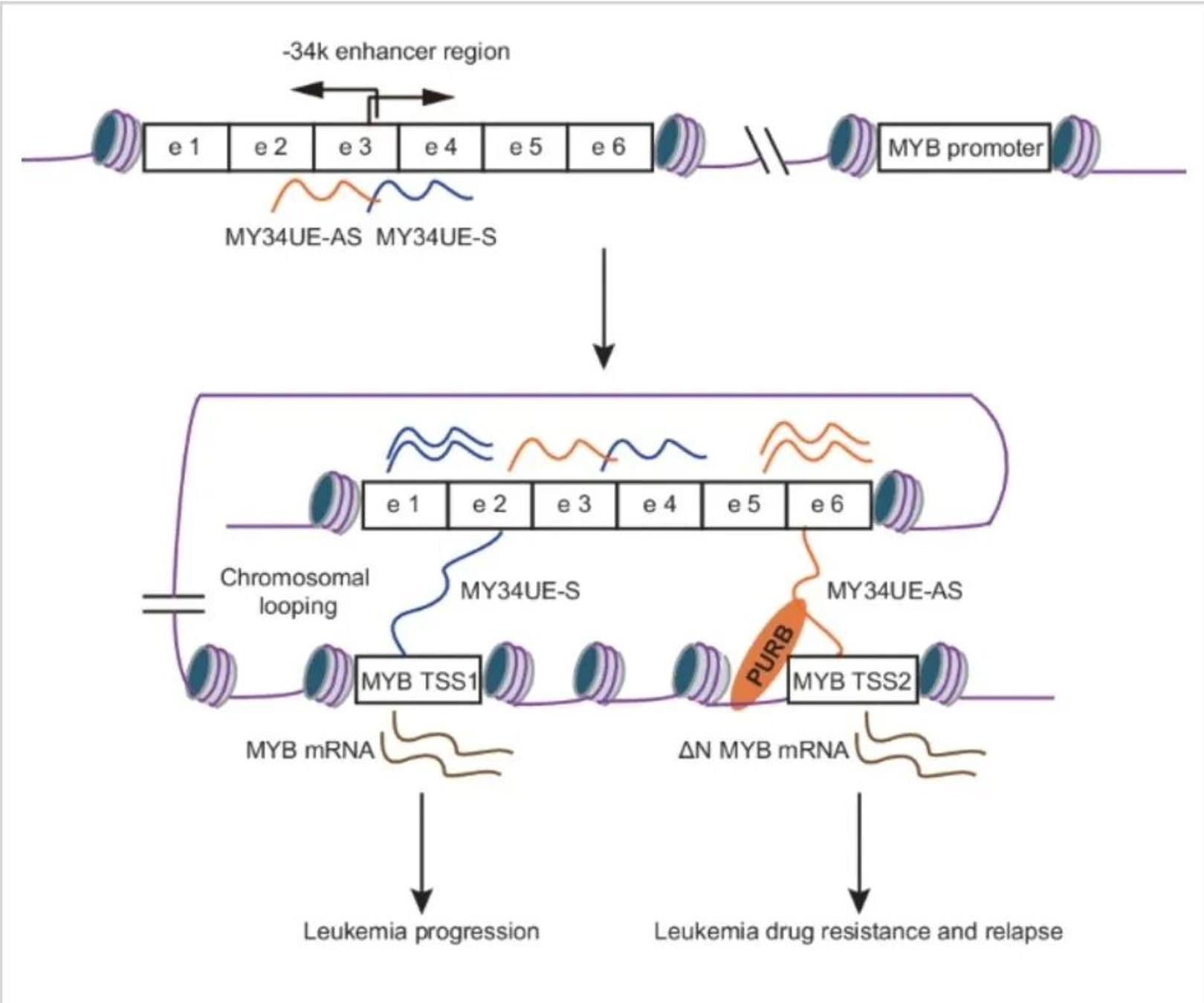
该研究首次鉴定出MYB上游-34 kb远端增强子双向转录的eRNAs:MY34UE-S和MY34UE-AS。研究发现,这两种eRNAs可选择性地与MYB基因的转录起始区域TSS1和TSS2的相互作用,从而转录出全长MYB和N端截短型MYB(ΔN MYB)。
作者还发现,两条eRNA分工不同:MY34UE-AS搭上PURB蛋白,把增强子和备用启动子拉到一起,生产短版MYB蛋白,导致耐药;而MY34UE-S负责连接增强子和经典启动子,生产正常MYB。我们可以把MYB基因想象成一个工厂的“生产线”。正常生产线(经典启动子)产出合格产品(全长MYB);而耐药细胞中,一条“非法改装线”(备用启动子)被激活,产出次品(短版MYB),导致产品失效(耐药)。而研究发现,MY34UE-AS就是启动这条“非法改装线”的罪魁祸首。
更重要的是,抑制MY34UE-AS,可以逆转耐药,且不影响正常MYB的生理功能。临床数据证实,这条通路的激活与患者复发和不良预后密切相关。这意味着,MY34UE-AS可以成为一个全新的耐药预测标志物和精准治疗靶点。这项研究为白血病精准治疗开辟了新路径,在揭示eRNA调控MYB基因启动子选择性使用的分子机制方面,具有原创性理论价值。
新医科研:医研融合、协同创新
以上三项研究均获得国家自然科学基金支持,体现了新疆医科大学“医研融合、协同创新”的鲜明特色。无论是脊柱外科团队立足临床需求,攻关仿生材料;还是心脏中心团队结合临床研究,为修复心肌损伤探索新路径,或是基础医学团队深入分子层面,破解耐药机制,成果的共同特点是:原创、深入、有临床转化潜力。这表明,我校正以多学科交叉、临床与基础并进的姿态,在科技创新的攻坚道路上发出属于新医的声音。
今后,我校将持续聚焦科技前沿和重大需求,加强基础研究,推动成果转化,深化科研组织模式,着力破解医药卫生领域的“卡脖子”难题。扎实推进有组织科研,培养高水平医学人才,助推新疆科技创新自立自强,以实际行动为“健康中国”建设贡献新医的智慧和力量。